Début 2023, l’équipe du Dr Thébaud a traité son premier patient dans le cadre d’un essai clinique visant à prévenir la dysplasie bronchopulmonaire chez les bébés prématurés. Il s’agit du premier essai clinique du genre au monde. Lisez l’entretien du Dr Thébaud pour en savoir plus sur son travail critique et ses motivations.
Publié : août 2020
La petite Olivia Eberts a eu des tubes d’oxygène dans le nez jusqu’après son premier anniversaire. Parce qu’elle est née prématurément, ses petits poumons n’étaient pas encore entièrement formés et elle ne pouvait pas respirer sans oxygène. Ironiquement, pour Olivia comme pour beaucoup d’autres bébés prématurés, l’oxygène qui lui a sauvé la vie a aussi endommagé ses poumons, la laissant avec une dysplasie bronchopulmonaire : l’équivalent d’une nouvelle vie marquée par l’emphysème. Cependant, un essai clinique mené à L’Hôpital d’Ottawa sous la direction du Dr Bernard Thébaud pourrait tout changer. Le traitement à base de cellules souches pourrait guérir les poumons des bébés prématurés.
Une naissance prématurée inattendue
Jamie Eberts, qui attendait des jumeaux, était enceinte de 22 semaines quand elle a commencé à ressentir de la douleur. À son arrivée au Campus Général de L’Hôpital d’Ottawa, elle a été hospitalisée : son travail avait commencé prématurément.
Heureusement, les médecins et les infirmières de L’Hôpital d’Ottawa étaient prêts à toute éventualité pour Jamie, son mari, Tim, et les bébés. Chaque jour, on discutait posément de l’état des bébés, de la façon de les mettre au monde et de leurs chances de survie. Chaque heure comptait. C’est alors que l’un des bébés a contracté une infection. Les trois vies étant en jeu, il fallait que Jamie accouche.
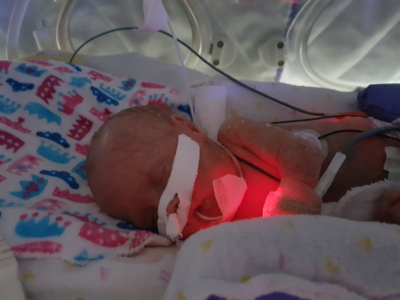
« Nos bébés, Liam et Olivia, sont nés à 5 heures du matin le 29 janvier 2017, à 23 semaines et demie de gestation. Liam est né en premier. Il était petit, rouge et ne faisait aucun son », se rappelle Jamie. Olivia pesait une livre et deux onces et Liam, seulement quelques onces de plus. Les deux bébés ont eu besoin d’oxygène et d’une ventilation artificielle pour rester en vie. Tous deux ont donc développé une dysplasie bronchopulmonaire — la cause de décès la plus courante chez les bébés prématurés.
Malheureusement, bébé Liam est décédé quelques semaines après sa naissance, tandis qu’Olivia a séjourné à l’Unité de soins intensifs néonataux (USIN) de L’Hôpital d’Ottawa pendant neuf longs mois.
La dysplasie bronchopulmonaire au Canada

Au Canada, 1000 bébés reçoivent un diagnostic de dysplasie bronchopulmonaire chaque année. Ils présentent bien souvent d’autres maladies pulmonaires chroniques, comme l’asthme, et bon nombre d’entre eux ont besoin d’un apport prolongé en oxygène et de ventilation. De plus, ils présentent dans bien des cas un taux élevé de réadmissions à l’hôpital pendant leurs deux premières années de vie. Les bébés atteints de dysplasie bronchopulmonaire ont souvent des problèmes qui touchent d’autres organes, dont le cerveau ou les yeux.
Quand Olivia a enfin pu sortir de l’hôpital, elle est rentrée chez elle branchée à une bonbonne d’oxygène. Au cours de sa première année de vie, elle a passé plus de temps à l’hôpital qu’à la maison.
« Même aujourd’hui, une simple grippe qui me cloue au lit pendant quelques jours lui vaut un séjour à l’hôpital et se transforme en pneumonie. C’est inquiétant », confie Jamie. Le docteur lui a dit qu’en raison de ses problèmes respiratoires, Olivia pourrait se retrouver très souvent à l’hôpital pendant toute sa vie.
Des possibilités de traitement limitées
À l’heure actuelle, il n’y a aucun traitement pour cette maladie », explique le Dr Bernard Thébaud, néonatologiste et chercheur principal à L’Hôpital d’Ottawa. Celui-ci est toutefois déterminé à changer les choses pour les bébés qui, comme Olivia, sont atteints de dysplasie bronchopulmonaire.
« Au laboratoire, nous avons découvert qu’un type particulier de cellules souches peuvent prévenir la dysplasie bronchopulmonaire ou régénérer les poumons des nouveau-nés. » — Dr Bernard Thébaud

« Dans nos recherches, nous utilisons des cellules souches isolées du cordon ombilical de nouveau-nés en santé, pour prévenir une lésion pulmonaire ou même dans une certaine mesure régénérer en laboratoire un poumon endommagé. Nous prévoyons que ces cellules souches, transplantées pendant un certain temps durant le séjour à l’hôpital des bébés, pourraient empêcher l’évolution de la maladie pulmonaire. »
Plutôt que de remplacer directement les cellules et les tissus endommagés comme le font les cellules souches habituelles, celles que le Dr Thébaud étudie produisent des facteurs de guérison qui favorisent la régénération et la réparation des cellules.
Un essai clinique porteur d’espoir
Le Dr Thébaud et son équipe de chercheurs ont lancé la première phase de l’essai clinique afin de vérifier la faisabilité et l’innocuité d’un traitement par cellules souches administré aux bébés prématurés. L’équipe fait tout en son pouvoir pour assurer le succès de cet essai clinique, notamment en consultant des professionnels de la santé et des parents de bébés prématurés.
Ces consultations leur ont appris, entre autres choses, que beaucoup de parents ont l’impression de ne pas en savoir assez sur les cellules souches et les essais cliniques pour décider s’ils veulent que leur enfant en fasse partie. Le Dr Thébaud et son équipe ont donc créé une vidéo animée qui explique ces concepts et aide les parents à prendre une décision éclairée. Les parents peuvent partager la vidéo avec des proches s’ils veulent un autre avis.
Jamie a participé à ces consultations et son expérience concrète a été très instructive pour l’équipe de recherche pendant la planification de ce projet. Voilà un exemple parmi tant d’autres qui illustre comment la collaboration entre les chercheurs de L’Hôpital d’Ottawa, les patients et leurs fournisseurs de soins améliorent la qualité et la réussite de la recherche.

Le Dr Thébaud et son équipe ont fait une « répétition générale » de leur essai clinique. « Cette répétition générale nous permet de tester et de perfectionner nos outils pour nous adresser aux parents, comme la vidéo, afin de savoir ce qui fonctionne le mieux quand nous serons prêts à commencer à offrir le traitement expérimental. »
Si ce premier essai est fructueux, le , Dr Thébaud et son équipe lanceront un essai clinique plus vaste au Canada. « Nous venons de franchir une étape décisive dans la mise au point d’un traitement révolutionnaire qui pourrait aider les bébés prématurés du Canada et du monde entier », affirme le Dr Thébaud.
L’essai clinique conçu à Ottawa est appuyé par le Centre de méthodologie et le Centre de fabrication de produits biothérapeutiques de L’Hôpital d’Ottawa, ainsi que par le groupe de recherche translationnelle Blueprint.
Un essai unique en son genre au Canada
« Les recherches sur les cellules souches sont incroyablement novatrices. Ici, nous disposons d’un nouveau traitement très prometteur qui pourrait prévenir une lésion pulmonaire et améliorer le développement du cerveau et la vision », déclare Janet Brintnell, gestionnaire clinique à l’USIN, qui a vu des dizaines de bébés prématurés atteints de dysplasie bronchopulmonaire.
« Quand on y pense, c’est incroyable ce que ce traitement pourrait faire pour donner une meilleure qualité de vie aux enfants et à leur famille et améliorer notre système de santé. Il pourrait réduire la durée des séjours et le nombre d’admissions à l’hôpital et améliorer les résultats à long terme. Il pourrait aider ces petits êtres à vivre en meilleure santé. » — Janet Brintnell
« Nous sommes les seuls à faire ce genre de recherches sur les cellules souches au Canada et seulement quelques équipes en font autant dans le reste du monde. » — Dr Bernard Thébaud
Pourtant, il y a trois ans, quand Olivia se trouvait à l’USIN, ce traitement n’était pas encore offert. Maintenant, Jamie et Tim encouragent les travaux du Dr Thébaud et sont optimistes quant à l’avenir des prochains bébés prématurés et de leur famille.
« Je crois que notre avenir est là, dit Jamie. Quand je pense à ce que ce traitement aurait pu faire pour notre famille, je me demande si Liam aurait pu survivre. Olivia ne vivrait peut-être pas avec les retards qu’elle connaît aujourd’hui. Même maintenant, si on nous demandait d’inscrire Olivia à l’essai clinique comme candidate plus âgée, nous le ferions. »
Jamie ajoute aussi que la maladie a eu des répercussions du point de vue de la santé mentale et des finances. « Les quatre premières années de la vie de notre aîné, Jacob, ont été très particulières parce qu’il a dû s’adapter énormément à cette situation difficile. Notre famille a aussi été mise à l’épreuve financièrement par toute cette expérience en raison des divers traitements dont Olivia a besoin. Nous avons dû apprendre à compter sur un seul revenu pendant plusieurs années pour gérer l’horaire complexe d’Olivia. Si nos jumeaux avaient eu accès aux recherches du Dr Thébaud à l’époque, nous aurions peut-être évité tout cela. »
Un nouveau départ
Olivia est maintenant une petite fille heureuse et active qui adore imiter son grand frère Jacob. Elle est toujours atteinte de dysplasie bronchopulmonaire, mais sa maladie est de plus en plus gérable et elle n’a plus besoin d’oxygène d’appoint. Olivia souffrira peut-être toute sa vie d’une maladie respiratoire, mais un jour, un traitement par cellules souches mis au point ici à Ottawa pourrait faire en sorte que la prochaine génération de bébés échappe à la dysplasie bronchopulmonaire.

Écoutez le balado Pulse et découvrez comment les cellules souches pourraient un jour guérir les poumons de bébés prématurés, avec le Dr Bernard Thébaud, et ce que cela pourrait représenter pour des parents comme Jamie Eberts.
Fièrement affilié à l’Université d’Ottawa, L’Hôpital d’Ottawa est un centre de recherche et de santé universitaire de premier plan.




