Publié : mai 2026
Temps de lecture : 4 min
Publié : mai 2026
Temps de lecture : 4 min
Olivier Duhaime a parcouru des centaines de kilomètres en Amérique du Nord. Il a participé à des ultramarathons et à quatre triathlons Ironman. Né à Montréal, Olivier a grandi à Hull, au Québec. Il est fier de sa province natale, tout en étant profondément attaché à la région de la capitale nationale — un attachement qu’il a célébré en parcourant à la course, sans assistance, les 400 kilomètres séparant l’Assemblée nationale du Québec de la Colline du Parlement à l’occasion du 150e anniversaire du Canada!
Depuis son premier marathon, qu’il a couru à 18 ans à peine, Olivier a toujours cherché à repousser ses limites. Mais à l’automne 2021, quelque chose a commencé à le ralentir. Une douleur sourde et persistante s’installait dans son dos. Au début, Olivier a essayé de l’ignorer. Comme beaucoup de sportifs, il avait l’habitude de surmonter la douleur. Mais il observait aussi l’apparition de symptômes étranges. Par exemple, une simple gorgée de bière le contraignait à s’allonger.
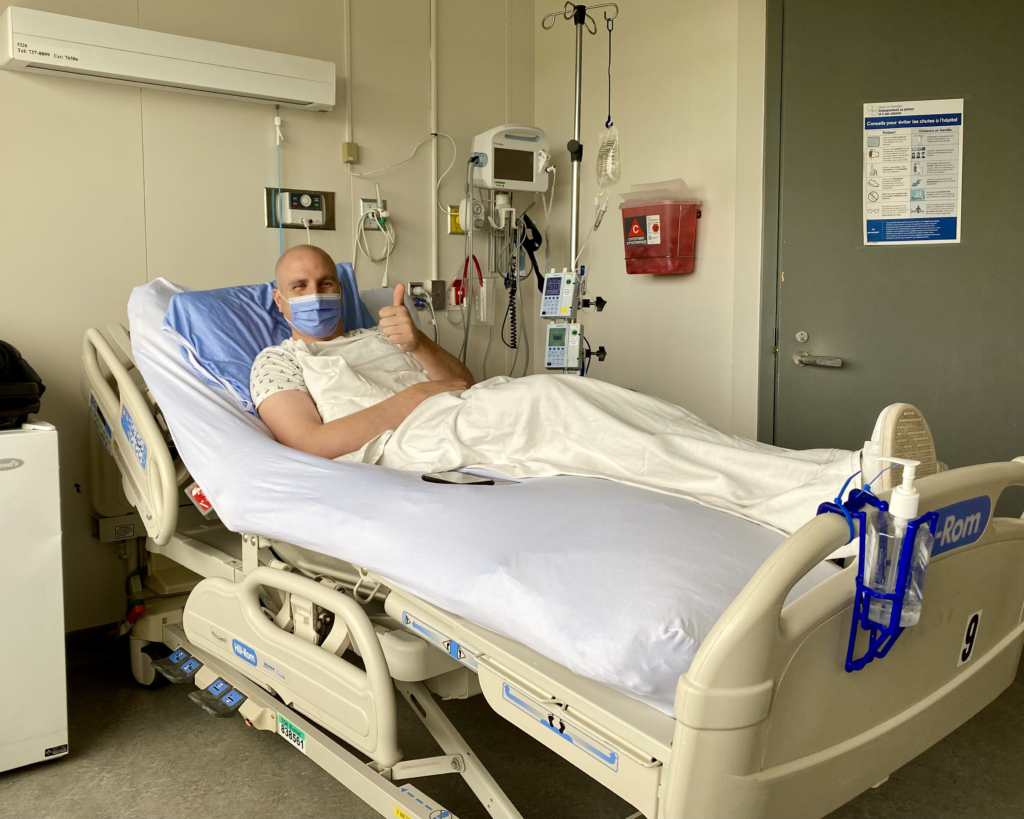
Au fil des mois, la douleur s’est intensifiée. « J’ai participé à des triathlons Ironman et à des ultramarathons. Je connais bien mon corps, explique Olivier. Je savais que quelque chose clochait. »
Pendant une nuit de février en 2022, la douleur est devenue insupportable. Olivier a décidé de se rendre en voiture à l’hôpital de Gatineau.
Ce qu’il était sur le point d’apprendre changerait sa vie à jamais.
« Je n’aurais jamais imaginé que cela puisse m’arriver. »
Les médecins ont demandé une tomodensitométrie, qui est un examen d’imagerie, afin de mieux comprendre l’origine des douleurs d’Olivier. Les résultats étaient bouleversants.
Les examens avaient décelé trois tumeurs : deux dans le dos d’Olivier et une près de sa poitrine. À seulement 32 ans, ce sportif d’endurance et père d’une petite fille de huit mois se retrouvait dans une situation pour lui inimaginable. Il avait un cancer.
À ce moment-là, tout ce qu’Olivier croyait savoir sur sa santé, son avenir et sa jeune famille a basculé. « Il n’y a aucun antécédent de cancer dans ma famille, explique-t-il. Je n’avais jamais vraiment pensé au cancer et je ne connaissais pas grand-chose sur le sujet. Je n’aurais jamais imaginé que cela puisse m’arriver. »
Le lendemain, sur le chemin du retour à la maison après son départ de l’hôpital, la réalité de son diagnostic s’imposa à lui. En voyant une petite fille qui patinait en plein air avec sa famille, Olivier ne put s’empêcher de se demander s’il serait encore en vie pour initier un jour sa propre fille au patinage.

Un diagnostic complexe
Au cours des jours suivants, Olivier subit une série d’examens et de biopsies afin d’aider les médecins à évaluer la maladie et à déterminer le meilleur traitement possible.
Les résultats allaient confirmer le diagnostic : un lymphome de Hodgkin de stade 4.
Olivier reçut une chimiothérapie au service de cancérologie de l’hôpital de Gatineau. Le traitement se révéla éprouvant physiquement et émotionnellement, mais les examens d’imagerie montreraient bientôt des résultats encourageants. Olivier entrevoyait une lueur d’espoir : il était en train de vaincre le cancer. Ce soulagement, toutefois, serait de courte durée.
À l’automne, des examens révélèrent que le cancer était revenu, plus fort et plus agressif qu’auparavant. Reconnaissant que l’état d’Olivier nécessitait un traitement hautement spécialisé, son équipe de soins l’orienta vers le Centre de cancérologie de L’Hôpital d’Ottawa, le chef de file régional de la prestation de soins avancés aux personnes cancéreuses et de la recherche sur le cancer.
Des soins spécialisés à L’Hôpital d’Ottawa
À L’Hôpital d’Ottawa, Olivier a été pris en charge par une équipe multidisciplinaire d’hématologues, d’infirmières et de spécialistes qui ont rapidement pris connaissance de ses examens d’imagerie, des résultats de ses biopsies et de l’information sur les traitements qu’il avait suivis afin d’élaborer un plan personnalisé, spécialement conçu pour traiter son lymphome agressif. Le plan de traitement comprenait une chimiothérapie intensive et une greffe de moelle osseuse réalisée par une équipe hautement spécialisée.
« Elle m’a dit : “Peut-être que dans d’autres hôpitaux, votre cancer serait considéré comme un cas compliqué. Mais ici, c’est quelque chose que nous traitons tous les jours.” C’est précisément à ce moment-là que j’ai retrouvé l’espoir. »
— Olivier Duhaime
Cette expertise a grandement rassuré Olivier.
« Je n’oublierai jamais l’infirmière qui m’a accueilli à mon arrivée à L’Hôpital d’Ottawa », raconte-t-il. À ce moment-là, il avait rédigé son testament, se préparant au pire. « Elle m’a dit : “Peut-être que dans d’autres hôpitaux, votre cancer serait considéré comme un cas compliqué. Mais ici, c’est quelque chose que nous traitons tous les jours.” C’est précisément à ce moment-là que j’ai retrouvé l’espoir. »
Olivier entama une chimiothérapie intensive, à raison de huit heures par jour pendant une semaine entière. Ce traitement allait le laisser épuisé, affaibli et totalement dépendant de son équipe de soins. Ça n’avait rien à voir avec la chimiothérapie qu’il avait reçue auparavant.

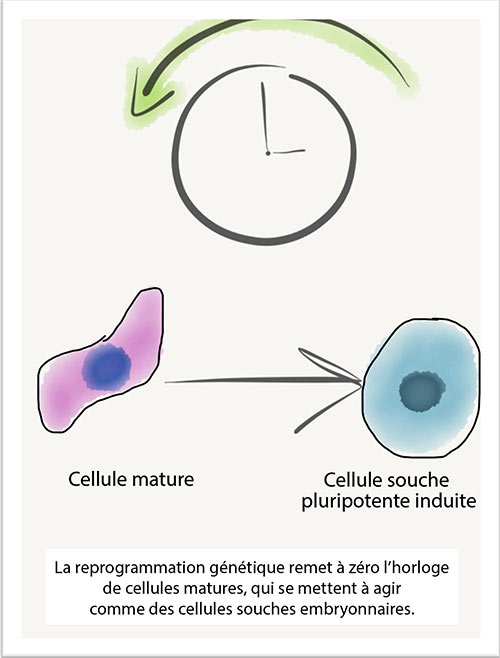
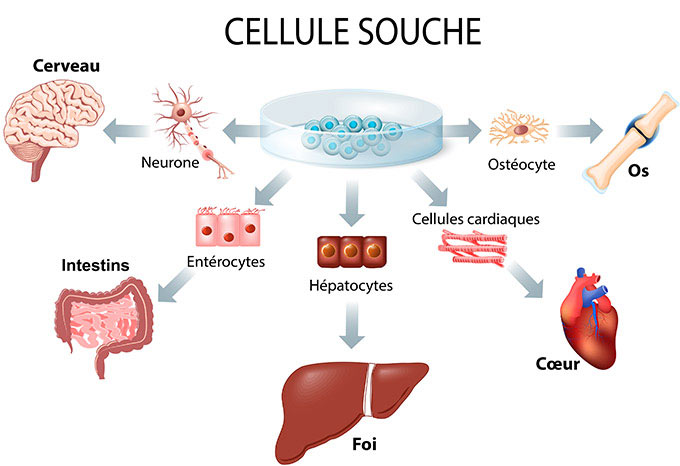
« La chimiothérapie à forte dose que nous administrons avant la greffe est très puissante et cible spécifiquement le lymphome, explique le Dr Ram Vasudevan, l’un des médecins responsables des traitements d’Olivier. Mais ce traitement détruit également la moelle osseuse. Nous réinjectons au patient ses propres cellules souches, qui agissent comme des graines. Elles trouvent le chemin de la moelle osseuse et commencent à régénérer le système sanguin et immunitaire du patient. Mais la période entre la chimiothérapie et la régénération de la moelle osseuse est très critique — en raison des complications liées à l’absence de moelle osseuse fonctionnelle, mais aussi des complications et des effets secondaires pouvant découler de la chimiothérapie à forte dose administrée au patient. »
C’était un traitement difficile, mais Olivier allait se découvrir une source de motivation inattendue dans son lit d’hôpital. Il savait que des coureurs se rassemblaient au centre-ville d’Ottawa pour le Fin de semaine des courses Tamarack d’Ottawa, l’un des plus grands événements de course à pied au pays, auquel il avait déjà participé. En regardant les coureurs franchir la ligne d’arrivée à la télévision, il se promit qu’un jour, il participerait de nouveau à cette course.
Tout sur l’activité physique et la santé mentale
Une seconde chance
Le 18 mai 2023, Olivier atteint ce que les équipes de greffe appellent le « jour 0 » : le jour où il allait recevoir ses cellules souches pour sa greffe de moelle osseuse. Les médecins ont injecté à Olivier ses propres cellules souches, qui se sont dirigées vers ses os et ont entamé l’extraordinaire processus de reconstruction de sa moelle osseuse et de son système immunitaire.
« Le jour 0 marque le début d’une toute nouvelle vie. »
— Olivier Duhaime
« Pour les patients greffés comme moi, c’est un jour très important. C’est une renaissance en quelque sorte, explique Olivier. Le jour 0 marque le début d’une toute nouvelle vie. »
Désormais, Olivier fête deux anniversaires : le premier est le jour de sa naissance, en mars, et le second, c’est le 18 mai – le jour où il a reçu sa greffe et une seconde chance de vivre.
Par la suite, son rétablissement a été lent et incertain. Son corps devait retrouver ses forces et rebâtir complètement son système immunitaire. Mais pas à pas – littéralement – Olivier retrouva son élan et put reprendre le cours de sa vie.
Et le jour tant attendu vint. Le jour où il pouvait recommencer à courir.
Redonner à l’Hôpital lors de la Fin de semaine des courses
La course à pied a toujours occupé une grande place dans la vie d’Olivier. Son retour à la course, même sur de courtes distances au début, avait pour lui une importance considérable.
Et comme il se l’était promis depuis son lit d’hôpital, ce printemps, Olivier courra le marathon de la Fin de semaine des courses Tamarack d’Ottawa. Cette fois-ci, il va courir pour une nouvelle raison : redonner à L’Hôpital d’Ottawa, qui lui a sauvé la vie. Olivier encourage ses amis, sa famille et la communauté tout entière à recueillir des fonds pour soutenir L’Hôpital d’Ottawa et les soins vitaux qu’il prodigue aux patients qui, comme lui, font face à un cancer.
« Je suis en vie aujourd’hui grâce à l’Hôpital et aux personnes qui l’appuient. »
— Olivier Duhaime
Gratitude et espoir
Ce printemps, Olivier et sa compagne, Justine, se préparent à accueillir leur deuxième enfant, un moment qu’Olivier a déjà pensé ne jamais pouvoir vivre.
De l’avis d’Olivier, s’il a pu reprendre le cours de sa vie, c’est grâce à l’expertise, à la compassion et au dévouement de son équipe de soins à L’Hôpital d’Ottawa, en particulier, l’équipe du Programme de transplantation et de thérapie cellulaire, et grâce à la générosité des donateurs.
« Je suis en vie aujourd’hui grâce à l’Hôpital et aux personnes qui l’appuient, dit-il. À chaque nouveau pas en avant, à chaque sortie de course, je songe avec reconnaissance à cette seconde chance qui m’a été donnée. »